ČLOVEK VERzUS BAKTÉRIE:
ÚLOHA
ANTIBIOTÍK
Ján Kormanec
Abstrakt. Baktérie ako najjednoduchšie živé organizmy na Zemi tu boli miliardy rokov pred nami. Sú prítomné vo všetkých možných lokalitách a sú schopné rásť pri rôznych podmienkach od mínusových teplôt až do 120 °C. Sú esenciálne pre život na našej planéte. Avšak sú rovnako aj zodpovedné za mnohé infekčné ochorenia. V priebehu histórie sa svety baktérií a človeka navzájom ovplyvňovali a bol to permanentný boj medzi nimi. V súčasnosti sa zdá, že najmä vďaka objavu antibiotík je človek čiastočne víťazom. Avšak vďaka jeho nezodpovednému správaniu sa je táto hrozba stále aktuálna.
Abstract. Man versus bacteria: the role of antibiotics. The simplest organisms on the Earth, bacteria, are billions years old. They were present in many various niches. They are able to grow in different conditions, high pressures in oceans, from minus temperatures to 120 °C. They are essential for the life of our planet. However, they are also responsible to many infection diseases. In the history, it was always a fight between a man and bacteria. Currently, a man, due to the discovery of antibiotics, is partially winning. But due to an irresponsible action of men, the threat is still here.
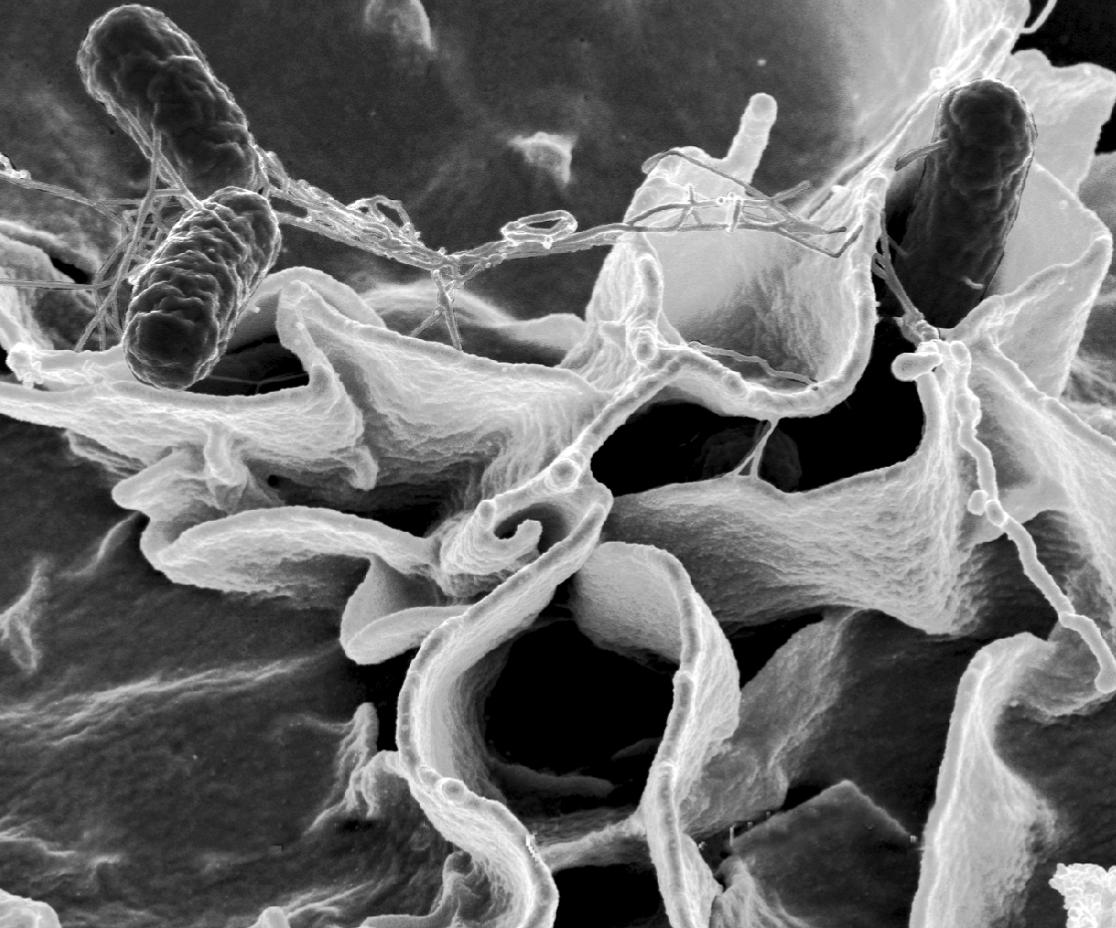
Pri pojme baktérie sa zrejme každému človeku vybavia najmä mnohé infekčné ochorenia, ktoré nás v priebehu nášho života postihujú. Skutočne, za veľkú väčšinu infekčných ochorení, ktoré nám znepríjemňujú život a v niektorých prípadoch hrozia aj smrťou, sú okrem vírusov zodpovedné malé mikroorganizmy – patogénne baktérie. Napriek tomu, že ich veľkosť je mnohonásobne menšia ako ktorákoľvek bunka nášho tela (obrázok 1), dokážu nám spôsobiť značné zdravotné komplikácie (napríklad za infekčné hnačkové ochorenia je v mnohých prípadoch zodpovedná baktéria Salmonella enterica) a niekedy nás dokážu aj zabiť.
Baktérie ako najjednoduchšie živé organizmy na Zemi tu boli miliardy rokov pred nami, sú všadeprítomné (napríklad v jednom grame pôdy ich je viac ako 109) a sú schopné života od mínusových teplôt až do 120 °C v horúcich prameňoch a pri vysokých tlakoch na dne oceánov. V rámci evolúcie sa svety baktérií a človeka navzájom ovplyvňovali, či už v pozitívnom alebo negatívnom zmysle slova, a človek, ako koruna tvorstva, sa tejto koexistencii musel prispôsobiť. Tisíce rokov ľudia nemali o baktériách ani poňatia a iba navonok pozorovali výsledky ich činností, produktom ktorých boli mnohé známe potraviny a nápoje. O objavenie baktérií ako príčiny ochorení sa až v polovici 19. storočia pričinili najmä dvaja vedci, Louis Pasteur a Robert Koch, ktorí dali základ aj vednej disciplíne, ktorá sa nimi zapodieva, mikrobiológii.
Avšak na baktérie sa nemôžeme pozerať ako na nevyhnutné zlo. Bez nich by život na Zemi nebol možný a človek je v mnohom na nich závislý. Tieto ľudskému oku neviditeľné tvory sú zodpovedné za kolobeh uhlíka, dusíka a ďalších prvkov na Zemi. Bez ich pôsobenia by sme mnohé veľmi chutné potraviny a nápoje ako napríklad jogurty, syry, čaj, kávu, víno, ani nepoznali. A rovnako nevyhnutná je ich činnosť priamo v našom organizme. V ľudskom tele sa nachádza viac než 200 druhov rôznych baktérií na rôznych miestach (napríklad na pokožke je ich okolo 1012, v čreve 1014 a v ústach 1010, takže oveľa viac ako všetkých buniek ľudského tela). Mnohé z nich majú pre človeka pozitívny význam, najmä v tráviacom trakte, kde tieto tzv. probiotické baktérie napomáhajú imunitnému systému, podporujú trávenie a produkujú pre človeka dôležité vitamíny. U prežúvavcov napomáhajú tráveniu pre nich nestráviteľnej celulózy z rastlín. Rovnako aj súčasný pokrok v biotechnológii využíva baktérie na produkciu mnohých biotechnologicky, ako aj klinicky dôležitých látok, ako sú vakcíny, liečivá, hormóny a enzýmy.
Napriek tomu sa pri pojme baktérie väčšine z nás vybaví najmä ich negatívny dopad na náš život vo forme mnohých infekčných ochorení. Čím sa tieto patogénne baktérie odlišujú od užitočných? Na rozdiel od mnohých neškodných baktérií, patogénne baktérie sú charakteristické určitými vlastnosťami, ktoré určujú ich patogenicitu alebo virulenciu (čiže schopnosť navodiť ochorenie), a to schopnosťou preniknúť do svojho hostiteľa (invazívnosť) alebo ho kolonizovať (parazitovať), schopnosťou odolávať obranným mechanizmom hostiteľa a produkciou toxických látok, ktoré poškodzujú hostiteľa. Dá sa povedať, že v priebehu našej koevolúcie s baktériami sme sa voči týmto malým nepriateľom vybavili mnohými obrannými systémami, najmä pre život nevyhnutným imunitným systémom, čo nás do istej miery chráni pred ich nepriaznivým pôsobením. Avšak história nás presviedča, že nie vždy sa nám v tejto vojne s mikrosvetom baktérii darilo, dôsledkom čoho sú mnohé známe prípady pandémií, kde mali tieto malé baktérie prevahu a v mnohých prípadoch boli zodpovedné za vyplienenie veľkej časti ľudskej populácie. Napríklad pandémia moru, tzv. „Čierna smrť“, za ktorú boli zodpovedné patogénne baktérie Yersinia pestis, v stredoveku vyplienila až tretinu európskej populácie a cholera i tuberkulóza, pôvodcami ktorých sú taktiež patogénne baktérie Vibrio cholerae a Mycobacterium tuberculosis, boli ešte koncom 19. storočia príčinou takmer 100 % úmrtnosti napadnutých osôb. Zastavenie týchto pandémií priniesol až revolučný objav antibiotík.
Prečo sú teda niektoré baktérie nebezpečné? Prečo počas evolúcie došlo k zmene nepatogénnych baktérií na nebezpečné patogény pre človeka a iné živočíchy? Čiastočnú odpoveď poskytujú výsledky výskumu dvoch vedných oblastí, a to molekulárnej biológie a genetiky, ktoré sa zapodievajú štúdiom života na molekulárnej úrovni. Pre lepšie pochopenie veľmi stručne vysvetlím základné princípy života a jeho fungovania. Základnou jednotkou života je bunka ako štruktúrna, funkčná, autonómne sa replikujúca jednotka každého živého organizmu. Poznáme bunky evolučne jednoduchšie, ako napríklad prokaryotické bunky baktérií, ktoré nemajú definované jadro, a bunky oveľa väčšie a komplikovanejšie, ako napríklad naše alebo rastlinné eukaryotické bunky s morfologicky definovaným jadrom. V každej bunke sa nachádza dlhá informačná molekula DNA, v ktorej sú zakódované informácie pre celý život bunky, pričom u eukaryotických buniek je DNA lokalizovaná v bunkovom jadre. Celý život každého živého organizmu je zakódovaný pomocou štvorpísmenkového kódu A G C T, zodpovedajúcemu základným výstavbovým prvkom (bázam) DNA, ktorými sú: adenín (A), guanín (G), cytozín (C) a tymín (T) umiestnené vo veľkej molekule DNA vo forme jej istých úsekov, tzv. génov. Avšak pre samotný život je nevyhnutný prepis tejto informácie (tzv. génová expresia) do 20-písmenkového kódu 20-tich rôznych aminokyselín v bielkovinách, ktoré sú základnými štruktúrnymi komponentmi bunky a zodpovedajú za všetky prejavy života (metabolizmus, rast, delenie atď). Tento geneticky kód sa prejavuje vo všetkých životných funkciách každého živého organizmu od baktérií až po človeka.
Po tomto stručnom úvode sa opäť vrátim k dôležitej otázke, prečo sú niektoré baktérie patogénne, a niektoré príbuzné nie. Rozhodujú o tom gény a ich expresia prispôsobená potrebám infekcie človeka a prežívania baktérie vo svojom hostiteľovi. Porovnanie sekvencií celých genómov (čo je kompletná molekula DNA obsahujúca všetky gény) mnohých patogénnych baktérií s genómami bezpečných bakteriálnych druhov, ako aj početné molekulárno-biologické štúdiá patogénnych baktérií odhalili mnohé tzv. gény patogenicity, ktoré sú zodpovedné za to, že tieto baktérie sú patogénne, a teda spôsobujú infekčné ochorenia. Takže o patogenicite rozhodujú tieto gény patogenicity a ich prepis (expresia) prispôsobený potrebám infekcie človeka a prežívania v ňom. Najnovšie poznatky preukázali veľmi sofistikované riadenie expresie génov patogenicity pre každé špecifické miesto infekcie v hostiteľovi, pre produkciu toxínov a dokonca pre ukrytie sa v imunitných bunkách, ktoré sú akoby „trójskym koňom“ umožňujúcim ich rozšírenie v celom organizme. Aby sme sa vedeli voči týmto nebezpečným multi-rezistentným baktériám brániť, musíme veľmi dobre poznať molekulové mechanizmy patogenicity a identifikovať analýzou týchto génov patogenicity najslabšie miesta v týchto baktériách, tzv. „ciele“ na ktoré je možné najefektívnejšie zaútočiť pri liečbe daného typu infekčného ochorenia. Voči takýmto „cieľom“, čo sú vo veľkej väčšine prípadov bielkoviny, ktoré sú produktom prepisu týchto génov, je po ich štruktúrnej analýze možné počítačovým modelovaním navrhnúť a následne pripraviť špecifické liečivá, ktoré by sa viazali na tieto „ciele“ a zamedzili tak rastu a infekčnosti dotyčnej patogénnej baktérie vo svojom hostiteľovi. Hoci je tento cielený výskum zatiaľ iba v počiatkoch, viaceré súčasné výsledky sú veľmi povzbudzujúce a naznačujú úspešnosť tohto prístupu, navyše aj s oveľa nižšou pravdepodobnosťou selekcie rezistentných baktérií voči takto pripravených liečivám. Preto aby sme sa vedeli voči týmto nebezpečným baktériám brániť, musíme ich veľmi dobre poznať. Boh nás stvoril na svoj obraz ako slobodné bytosti a venoval nám svoje dielo, aby sme ho spoznávali a zodpovedne užívali.
Zastavenie pandémií, ktoré plienili ľudskú populáciu, priniesol až revolučný objav antibiotík v prvej polovici dvadsiateho storočia, a to najmä zásluhou Alexandra Fleminga a jeho náhodného objavu penicilínu, ktorý odštartoval rozmach vedeckého bádania v oblasti produkcie antibiotík, kulminujúci zlatou érou antibiotík v období rokov 1945 až 1960. Či si to uvedomujeme alebo nie, tieto úžasné magické guľôčky („magic bullets“) ako ich nazval jeden z priekopníkov ich výskumu Paul Ehrlich, zachránili milióny ľudských životov. V súčasnosti je známych viac než 15 000 rôznych antibiotík, avšak iba malé percento z nich má aj uplatnenie v klinickej praxi pri liečbe infekčných ochorení. Antibiotiká sú nízkomolekulové látky (obrázok 2), produkované baktériami a plesňami.
Pôsobia dominantne selektívne baktériostaticky (zastavujú rast) alebo baktériocidne (zabíjajú bunky) iba na baktérie. Veľké množstvo objavených antibiotík je však nepoužiteľné kvôli ich vysokej toxicite aj voči ľudskému organizmu a iným zlým vlastnostiam. Avšak pomocou genetických manipulácií s génmi zodpovednými za produkciu týchto antibiotík je už v súčasnosti možná príprava alebo modifikácia antibiotík s lepšími vlastnosťami pre liečbu infekčných ochorení.
Obdobne ako je to s každým objavom človeka, tak aj v prípade antibiotík ich nesprávne používanie, dávkovanie, zbytočná antibiotická liečba vírusových ochorení, použitie antibiotík ako rastových stimulátorov v živočíšnej výrobe (v EU je v súčasnosti už zákaz pre takéto použitie, pričom v USA stále ešte nie!) sa obrátilo proti ľudom a spôsobilo selekciu tzv. multi-rezistentných baktérií, voči ktorým sme viac-menej bezmocní a v súčasnosti sú skutočnou hrozbou pre ľudskú populáciu. Je pochopiteľné, že baktérie sa voči antibiotikám bránia a sporadicky, či už mutáciami v ich génoch alebo veľmi frekventovaným tzv. horizontálnym prenosom génov (akýmsi rýchlym požičaním) potrebných na prežitie v prítomnosti antibiotík, sa v populácii v malej miere vyselektujú aj rezistentné formy patogénnych baktérií na používané antibiotikum. Všetky už spomenuté negatívne ľudské zásahy túto selekciu dramaticky urýchlili a v nemocniciach sa sporadicky objavujú patogénne baktérie obsahujúce mnohé gény rezistencie voči bežne používaným antibiotikám, proti ktorým nemáme na trhu žiadne účinné antibiotikum, hoci v klinickej praxi sú ich stovky. Na dôvažok, v súčasnosti mnohé farmaceutické firmy prestali vyvíjať nové antibiotiká pre liečbu infekčných ochorení, keďže sa riadia čisto ekonomicky a tento typ produkcie je pre nich nerentabilný, lebo ich potreba pre pacientov je iba sporadická a v relatívne krátkom čase infekčného ochorenia. Radšej preorientovali svoj výskum na chronické a iné ochorenia, kde je nutné dlhodobé používanie liečiva. Preto sú neustále sa objavujúce multi-rezistentné baktérie a dramatický pokles v zavádzaní nových účinných liečiv na liečbu infekčných ochorení tikajúcou bombou, ktorú si uvedomujú aj mnohé vedecké a klinické inštitúcie, a bijú na poplach. Tieto výzvy našťastie v posledných rokoch našli určitú odozvu, odrazom čoho je rast podpory výskumu v tejto oblasti s dôrazom na nové inovatívne postupy. Okrem klasického skríningu toho, čo nám príroda ponúka vo forme prírodných produktov antibiotík produkovanými mnohými najmä pôdnymi baktériami a plesňami, čo je cesta zdĺhavá a ekonomicky náročná, dramatický prienik moderných vedeckých disciplín molekulovej biológie a genetiky do tejto oblasti dáva pozitívne vyhliadky na riešenia tohto akútneho problému. Ako som už uviedol, najnovšie poznatky preukázali veľmi sofistikované riadenie expresie génov patogenicity pre každé špecifické miesto infekcie v hostiteľovi, pre produkciu toxínov a dokonca pre ukrytie sa v imunitných bunkách (kde sú akoby „trójskym koňom“ umožňujúcim ich rozšírenie v celom organizme). Ak sa chceme vedieť brániť voči týmto nebezpečným multi-rezistentným baktériám, musíme rovnako aj veľmi dobre poznať molekulové mechanizmy patogenicity a analýzou génov patogenicity identifikovať najslabšie miesta v týchto baktériách, ako som to uviedol v predchádzajúcej časti. Takže v budúcnosti budeme zrejme bojovať proti baktériám liečivami, ktoré budú oveľa účinnejšie ako dnešné antibiotiká a zároveň bude výrazne znížená pravdepodobnosť selekcie baktérií rezistentných voči takto pripraveným liečivám. Veľmi nádejným prístupom pri príprave nových účinných antibiotík založeným na technikách molekulovej biológie je takzvaná „kombinačná biosyntéza“ antibiotík. Prírodné antibiotiká sú syntetizované veľkým komplexom mnohých enzýmových bielkovín, z ktorých každá uskutoční jednu chemickú reakciu vedúcu k výslednej štruktúre molekuly antibiotika. Všetky tieto enzýmy sú kódované génmi, ktoré sú usporiadané v dlhých úsekoch zvaných „klastre“. Klastre génov mnohých v prírode vytváraných antibiotík boli identifikované a spoľahlivo charakterizované. S využitím tejto informácie boli potom sofistikovaným zmiešaním génov z rôznych antibiotikových klastrov pripravené úplne nové klastre. Tieto klastre boli následne zavedené do produkčných baktérií a tieto baktérie začali produkovať úplne nové, v prírode sa nevyskytujúce antibiotiká. V súčasnosti sú známe už stovky takýchto antibiotík a mnohé z nich majú veľmi účinné vlastnosti pri liečbe infekčných, ako aj nádorových ochorení. Viaceré z týchto látok sú už dokonca v jednotlivých etapách klinických testov pre ich zavedenie do klinickej praxe. Takže ostáva nám dúfať, že spojeným úsilím mnohých vedcov, ako aj niektorých farmaceutických firiem sa aj s týmto problémom v budúcnosti úspešne vyrovnáme.
Na záver si pomôžem optimistickým citátom z Biblie: „A Boh videl všetko, čo urobil, a hľa, bolo to veľmi dobré. A nastal večer a nastalo ráno, deň šiesty“ (Gn 1, 31). Takže ako som sa snažil v tomto článku naznačiť, aj baktérie majú svoje veľmi dôležité miesto na tomto svete, ale ako je to už v priebehu celej existencie ľudstva, nezodpovedná a niekedy až egoistická činnosť človeka nám často spôsobuje vo veľkej miere problémy.
Podrobnejšie informácie o nových prístupoch k antibiotikám nájde čitateľ napr. v [1-2, 4-6].
Literatúra
[1] DEMAIN, A. L.: Antibiotics: Natural products essential to human health. In: Medicine Res. Rev. 2009, roč. 29, s. 821 – 842.
[2] DEMAIN, A. L., SANCHES, S.: Microbial drug discovery: 80 years of progress. In: J. Antibiot. 2009, roč. 62, s. 5 – 16.
[3] http://www.fr.academic.ru/pictures/frwiki/83/SalmonellaNIAID.jpg
[4] OCHI, K., HOSAKA, T.: New strategies for drug discovery: activation of silent or weakly expressed microbial gene clusters. In: Appl. Microbiol. Biotechnol. 2013, roč. 97, s. 87 – 98.
[5] MITCHELL, W.: Natural products from synthetic biology. In: Curr. Opin. Chem. Biol. 2011, roč. 15, s. 505 – 515.
[6] VICENTE, M., HODGSON, J., MASSIDA, O., TONJUM, T., HENRIQUES-NORMARK, B., RON, E. Z.: The fallacies of hope: will we discover new antibiotics to combat pathogenic bacteria in time? In: FEMS Microbiol. Rev. 2006, roč. 30, s. 841 – 852.

Obrázok 1. Patogénna baktéria Salmonella enterica (malé oválne bunky vľavo hore) infikuje povrch epitelovej bunky tenkého čreva [3].
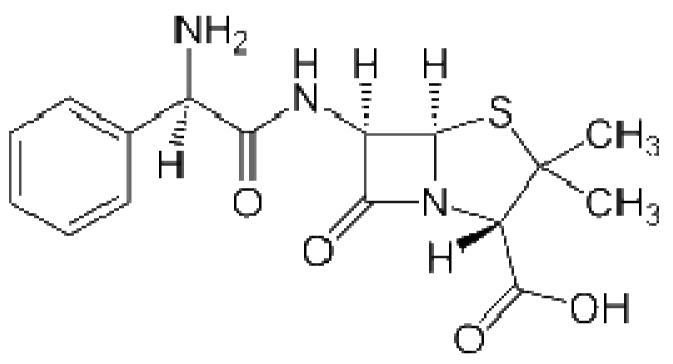
Obrázok 2. Štruktúrny vzorec antibiotika ampicilínu.